Kalijum permanganat
| Kalijum permanganat | |||
|---|---|---|---|
 | |||
 | |||
| IUPAC ime |
| ||
| Drugi nazivi | Kalijum hipermangan, kameleonski mineral, Kondijev kristal | ||
| Identifikacija | |||
| CAS registarski broj | 7722-64-7  Y Y | ||
| PubChem[1][2] | 516875 | ||
| ChemSpider[3] | 22810  Y Y | ||
| EINECS broj | 231-760-3 | ||
| UN broj | 1490 | ||
| KEGG[4] | D02053 | ||
| RTECS registarski broj toksičnosti | SD6475000 | ||
| ATC code | D08AX06,V03AB18 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | KMnO4 | ||
| Molarna masa | 158.04 g/mol | ||
| Agregatno stanje | purpurnobronza sivi kristali; ciklamacrveno u rastvoru | ||
| Gustina | 2.703 g/cm³, osnovno | ||
| Tačka topljenja | 270 °C razgrađuje se | ||
| Rastvorljivost u vodi | 6.38 g/100 ml na 20 °C | ||
| Struktura | |||
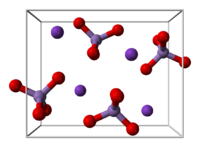
| Kristalna rešetka/struktura | ortorombična struktura | ||
| Termohemija | |||
| Standardna entalpija stvaranja jedinjenja ΔfH | -813.4 kJ.mol-1 | ||
| Standardna molarna entropija S | 171.7 J.K-1.mol-1 | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | External MSDS | ||
| Opasnost u toku rada | Oksidant (O), Škodljiv (Xn), Opasan po životnu sredinu (N) | ||
| NFPA 704 |  0 1 3 OX | ||
| R-oznake | R8, R22, R50/53 | ||
| S-oznake | S2, S60, S61 | ||
| Srodna jedinjenja | |||
| Drugi katjoni | Natrijum-permanganat | ||
| Srodna jedinjenja | Natrijum-permanganat (K2MnO4); Mangan-heptoksid; | ||
|
| |||
| Infobox references | |||
Kalijum permanganat (latinski kalium hipermanganicum) je neorgansko hemijsko jedinjenje koje spada u grupu kalijumovih soli. Molekulska formula kalijum permanganata je KMnO4.[5][6]
Pri normalnim uslovima nalazi se u čvrstom agregatnom stanju i ima gustinu 2,7 g/cm3. Gradi karakteristične plavo-ljubičaste kristale. Dosta loše se rastvara u vodi (na temperaturi 20 °C 6,4 g u 100 cm³). Na temperaturi preko 230 °C razlaže se po formuli:
- 2KMnO4 → K2MnO4 + MnO2 + O2
Kalijum permanganat je jak oksidans. Reakcija dosta zavisi od pH vrednosti rastvora. U kiselim rastvorima podleže redukciji do slabo obojenog mangan(II):
- MnO4- + 8H+ + 5e- → Mn2+ + 4H2O
U slabim baznim i neutralnim rastvorima redukuje se do mangan dioksida, koji se izdvaja iz rastvora u obliku braon taloga:
- MnO4- + 2H2O + 3e- → MnO2 + 4OH-
Dok se u jako baznim rastvorima redukuje do zelenog mangana (VI):
- MnO4- + e- → MnO42-
Kalijum permanganat poseduje jake baktericidne (ubija bakterije) osobine. Zbog toga se koristi za prečišćavanje vode za piće, u mastima za dezinfekciju grla i u preparatima za dezinfekciju rana.
Vodeni rastvori kalijum permanganata u zavisnosti od koncentracije poseduju boju od svetlo crvene do tamno ljubičaste, pri čemu se boja pojavljuje već pri veoma malim količinama ovog jedinjenja.
Molarna masa kalijum permanganata je 158.04 g/mol
Vidi još
Reference

- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519. edit
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846. edit
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Housecroft C. E., Sharpe A. G. (2008). Inorganic Chemistry (3rd izd.). Prentice Hall. ISBN 978-0-13-175553-6.
- ↑ Holleman A. F., Wiberg E. (2001). Inorganic Chemistry (1st edition izd.). San Diego: Academic Press. ISBN 0-12-352651-5.
Spoljašnje veze
 | Portal Hemija |
- p
- r
- u





